La Agencia Europea de Medicamentos (EMA) permitió que los estados miembros utilicen la píldora contra el COVID-19 de Pfizer, antes de su aprobación formal, y autorizó dos tratamientos más, en su lucha contra el aumento de contagios.
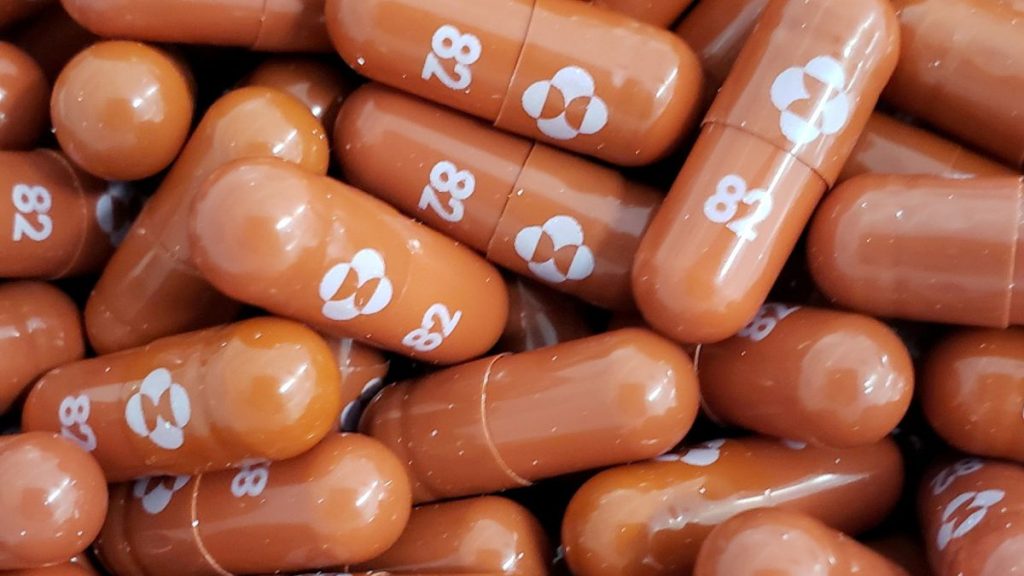
La píldora de Pfizer, al igual que la de su rival Merck (con una aprobación de emergencia de la EMA), no necesitan inyección o entrada por vía intravenosa, por lo que son más accesibles.
El gigante farmacéutico Pfizer indicó esta semana que la píldora, que reduce las hospitalizaciones y las muertes de personas de riesgo en un 90%, debería resistir a la nueva variante del COVID, Ómicron.

El fármaco, que aún no está autorizado en la UE, puede utilizarse para tratar a los adultos con COVID-19 que no requieren oxígeno suplementario y que tienen un mayor riesgo de desarrollar una forma grave de la enfermedad”, dijo la EMA en un comunicado.
La agencia explicó que emitió esta recomendación para apoyar a las autoridades nacionales que puedan decidir una utilización anticipada del medicamento, por ejemplo ante un alza de los contagios y las muertes por COVID-19 en la Unión Europea.
Este tratamiento, denominado Paxlovid, es una combinación de una nueva molécula, el compuesto PF-07321332 y el antiretroviral ritonavir, que se utiliza contra el virus del sida.

Para el dirigente de Pfizer, Albert Bourla, Paxlovid “si se autoriza, tiene potencial para ayudar a salvar vidas y reducir las hospitalizaciones”, explicó en un comunicado.
“Paxlovid debería ser administrada lo antes posible tras el diagnóstico del COVID-19 en los cinco primeros días desde el inicio de los síntomas”, indicó la EMA que agregó que el tratamiento debe extenderse durante cinco días más.
Los efectos secundarios más corrientes son perturbaciones en el gusto, diarrea y vómitos. Este compuesto no debe ser administrado a mujeres embarazadas y la lactancia debe ser interrumpida, en caso de su utilización.
La EMA lanzó el 13 de diciembre un examen acelerado de una autorización de comercialización.
Dinamarca aprueba píldora de Merck
Dinamarca se convirtió el jueves en el primer país de la UE en autorizar el uso de la píldora de Merck, autorizada por la EMA en noviembre. Sin embargo, los resultados clínicos publicados por Merck fueron decepcionantes ya que mostraban menos eficacia que en anteriores ensayos (a partir de resultados provisionales).
Por otro lado, la EMA aprobó hoy dos fármacos, el Xevudy de GlaxoSmithKline, y el tratamiento Kineret, de Orphan Biovitrum, para pacientes con riesgo de desarrollar complicaciones graves del COVID-19.
AFP
Elija a Q’HUBO Bogotá como su fuente de información preferida en Google Noticias aquí.
¿Qué tal le pareció este contenido?
¡Haga clic en una estrella para puntuar!
Promedio de puntuación 0 / 5. Recuento de votos: 0
Hasta ahora, ¡no hay votos!. Sea el primero en puntuar este contenido.

















